Vấn đề Botox và bệnh viện thẩm mỹ nâng ngực
Vấn đề dược chất sinh học dùng vào mục đích thẩm mỹ cũng được xét duyệt gắt gao như việc cấp phép phẫu thuật nâng ngực cấy ghép
Hiệp hội dược phẩm đề xuất với Bộ An toàn Thực phẩm và Dược phẩm rằng “Botox xuất khẩu gián tiếp, nên miễn xét duyệt lô hàng”
Trong khi các công ty sản xuất chất botulinum lớn như Medytox và Hugel đang đấu tranh với chính phủ về tính hợp pháp của việc bán các mặt hàng xuất khẩu gián tiếp sang Hàn Quốc mà không được chấp thuận cho việc vận chuyển từ nhà nước, Hiệp hội Công nghệ Sinh học và Dược phẩm Hàn Quốc bắt đầu hỗ trợ các công ty.
Theo ngành công nghiệp dược phẩm và sinh học ngày 30, Hiệp hội Dược phẩm và Công nghệ Sinh học Hàn Quốc mới đây đã báo cáo Bộ An toàn Thực phẩm và Dược phẩm (MFDS), "Xuất khẩu gián tiếp các công thức độc tố botulinum thông qua các công ty thương mại trong nước cũng là xuất khẩu. Vì vậy nó có đã được phê duyệt cho việc vận chuyển mặt hàng trên toàn đất nước Hàn Quốc, nên được miễn trừ. "
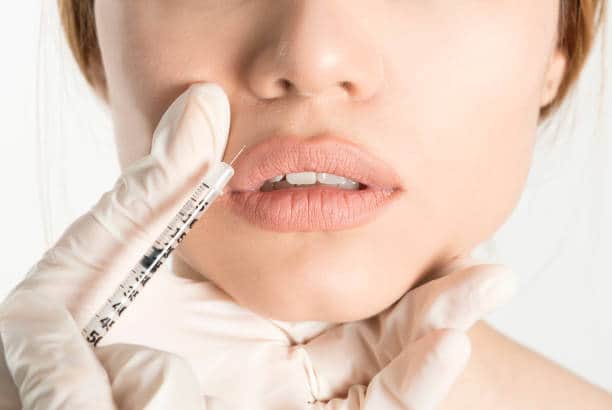
Công thức Botulinum, còn được gọi là 'Botox', là dược phẩm sinh học chủ yếu được sử dụng cho phẫu thuật thẩm mỹ như cải thiện nếp nhăn giữa lông mày.
Để bán các sản phẩm sinh học như botulinum ở Hàn Quốc, ngay cả khi họ đã nhận được phê duyệt trước về sản phẩm, họ phải có được phê duyệt lô hàng quốc gia riêng từ Bộ An toàn Thực phẩm và Dược phẩm để kiểm tra chất lượng của chúng.
Bộ An toàn Thực phẩm và Dược phẩm đã hủy bỏ giấy phép sản phẩm cho Medytox vào tháng 10 năm 2020, các chế phẩm chứa độc tố botulinum của Hugel và Pharma Research Bio vào tháng 12 năm 2021 vì họ không nhận được phê duyệt lô hàng quốc gia.
Các công ty này đang có quan điểm rằng các sản phẩm bị Bộ An toàn Thực phẩm và Dược phẩm tiêu hủy không phải được phê duyệt lô hàng quốc gia vì chúng là thuốc được sản xuất có dùng trong thẩm mỹ và bán để xuất khẩu. Có ý kiến cho rằng Bộ An toàn Thực phẩm và Dược phẩm đã giải thích các sản phẩm thẩm mỹ xuất khẩu thông qua các công ty thương mại được thành lập tại Hàn Quốc là 'bán hàng nội địa'.
Medytox, Hugel và Pharma Research Bio đã đệ đơn kiện hành chính lên Bộ An toàn Thực phẩm và Dược phẩm, trì hoãn hiệu lực của việc hủy bỏ giấy phép sản phẩm sau ngày phán quyết về vụ việc ban đầu và tiếp tục sản xuất và bán hàng.